Chemische Reaktionen
Probetest: hier
Aufgaben:
Darstellung von chemischen Reaktionen
a) Was sind Edukte?
b) Wann nennt man eine Reaktion reversibel?
Massenerhaltung
a) Unter welchen Bedingungen kann man das
Massenerhaltungsgesetz
experimentell
nachweisen?
b) Erklären Sie das Massenerhaltungsgesetz mit
Hilfe des Teilchenmodells.
Ausbalancieren von
Reaktionsgleichungen
Ergänzen
Sie diese unvollständigen Reaktionsgleichungen:
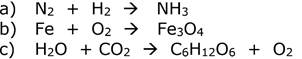
Mengenverhältnisse
Sie wollen 3 mol
Kochsalz aus Chlor und Natrium herstellen.
a) Stellen
Sie die Reaktionsgleichung dazu auf.
b) Wieviel
Chlor und wieviel Natrium müssen sie dazu nehmen?
(Angabe in mol und in
Gramm jeweils auf 2 Stellen nach dem Komma)
Die Reaktionsgleichung der Zellatmung
enthält Glucose (C6H12O6) und
Sauerstoff (O2) als Edukt und
Wasser und Kohlendioxid als Produkte.
c) Stellen
Sie die (vollständige) Reaktionsgleichung auf.
d) Wieviel
Wasser entsteht bei der Veratmung von 100 g Glucose?
(auf 1 Stelle nach dem Komma)
Sie möchten 10 g TNT aus Toluol (ein
Lösungsmittel) und Kaliumnitrit
(Dünger) herstellen? Kaliumnitrit kennen
Sie vom Kap. 9.1.
Toluol hat die Strukturformel: TNT diese:
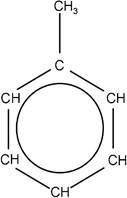
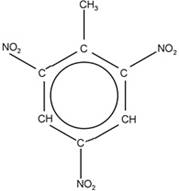
e)
Notieren Sie sich zuerst die Summenformel von
Toluol, Kaliumnitrit und TNT.
f)
Stellen Sie die Reaktionsgleichung auf (als zweites
Produkt entsteht KH).
g) Rechnen
Sie die Molekülmassen für Toluol und für TNT aus.
h) Wieviel
Toluol brauchen Sie dazu (auf 2 Stellen genau)?
i) Wieviel
Kaliumnitrit brauchen Sie dazu (auf 2 Stellen genau)?
j) Wie viele Gew-% sind
12 g Glucose in 1 kg Lösung?
k) Wie viele Vol-% hat
eine Alcopop, bei dem 2,4 dl Industrie-
ethanol pro Liter Getränk dazugemischt
wurde?
(Volumenkonzentration
nicht berücksichtigen)
l) Wie stellt man 2 dl einer wässrigen
Natriumhydroxid-Lösung mit
ca.
15 Gew-% her?
m) Wie stellt man 2 dl einer wässrigen
Natriumhydroxid-Lösung mit
genau
15 Gew-% her?
n) Wie viele Vol-%
Ethanol hat eine Mischung aus 32 ml Ethanol und
100
ml Wasser?
(Volumenkonzentration nicht
berücksichtigen)
o) In
einem Messzylinder werden 1 ml Methanol mit Wasser bis zur
100 ml-Marke aufgefüllt (Methanol: ρ=0,793 g/ml). In einem anderen
Messzylinder werden 2 g Nicotin (C10H14N2)
in 100 ml Wasser aufgelöst.
Wie gross sind die Molaritäten der
beiden Lösungen?
p) Wie
gross ist die Molarität von reinem Wasser?
Energiebetrachtung
a) Was ist die Aktivierungsenergie (Definition)?
b) Setzen Sie die Aktivierungsenergie in einen
Zusammenhang mit
anderen
Energien.
c) Was ist eine endotherme Reaktion
(Definition)?
d) Wie kann man eine endotherme Reaktion im
Labor wahrnehmen?
Energieerhaltung
a) Wie lautet das Gesetz der Energieerhaltung?
b) Worin wird die Energie gespeichert, die bei
einer endothermen
Reaktion
der Umgebung entzogen wird?